实验室在微创植入式柔性深脑区脑机接口方面取得进展
近日,中国科学院上海微系统与信息技术研究所周志涛研究员团队与上海脑虎科技有限公司陶虎研究员团队合作,开发出蚕丝蛋白赋能的微创植入式脑室内柔性神经界面,可在脑脊液环境中自展开,适形贴附于深脑核团及脑室等大脑“内表面”并长期在体监测,为深脑核团相关神经疾病的解析提供了一种全新的技术手段。相关研究成果以“Silk-enabled Conformal Intraventricular Interfaces for Minimally Invasive Neural Recordings”为题于2025年10月23日发表于国际学术期刊《自然•通讯》(Nature Communications)(DOI: 10.1038/s41467-025-64397-9)。
深部脑结构(丘脑、基底节、边缘系统、脑干和小脑等)在认知、情绪和运动等功能中发挥关键作用,其中脑室周结构及功能异常与帕金森病、阿尔茨海默病、抑郁和孤独症等多种疾病密切相关。现有柔性平面电极虽具大覆盖与高贴附的优势,但难以微创植入大脑的“内表面”;而SEEG、Neuropixels等穿刺式神经电极可达深脑,却可能对目标核团造成侵袭,且在动态脑脊液环境下进行大面积、低损伤、长期监测仍面临挑战。因此,构建一种与微创神经外科流程相兼容、可在脑室内稳定贴附并实现高信噪比监测的柔性神经界面,具有重要的基础研究与临床转化意义。
针对上述需求,研究团队创新性地提出形状记忆丝蛋白支架结合可变形微电极阵列的神经界面方案:可微型化装配于临床常用规格微创手术导管实现微创递送;进入侧脑室后凭借丝蛋白支架的形状记忆功能实现自展开与适形贴附;电极走线层引入共面金属屏蔽以抑制工频噪声干扰,保障在复杂手术环境与长期随访中的信号质量。团队在帕金森绵羊中完成术中与自由活动状态下的在体验证,神经界面在绵羊尾状核头表面实现稳定记录,成功捕捉到帕金森病相关β振荡以及对左旋多巴干预的响应,并在为期四周的慢性记录中维持良好电学性能与组织相容性,展示出面向深脑及脑室通路的微创、长期、广覆盖神经环路监测能力(图1)。
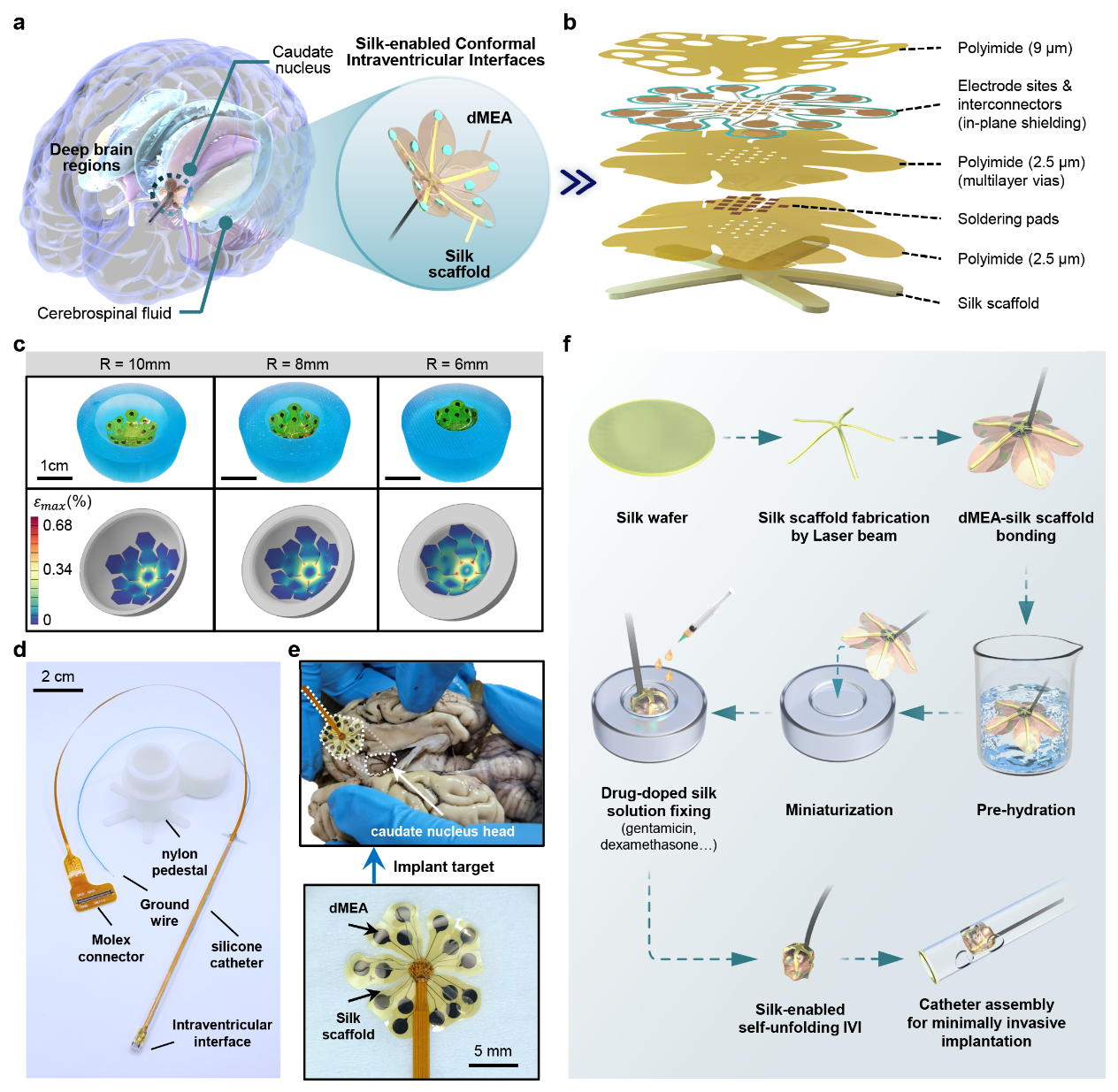
图1. 丝蛋白赋能微创植入式脑室内柔性神经界面总体概览:微创递送与自展开贴附示意、器件爆炸图、曲面适形有限元仿真与实物验证、系统实物、可变形微电极与丝蛋白支架,以及微创植入界面器件的集成。
该论文第一作者为上海微系统所博士生梁佶智和博士后王馨儿,通讯作者为上海微系统所周志涛研究员、脑虎科技陶虎研究员。中国科学院上海微系统与信息技术研究所为该研究第一完成单位和通讯单位,合作单位包括复旦大学附属华山医院等。该研究工作得到了中国科学院青年创新促进会优秀会员(Y2023070)、上海市基础研究特区计划(JCYJ-SHFY-2022-01)、国家自然科学基金(52371249)等项目的支持。
论文链接:https://www.nature.com/articles/s41467-025-64397-9